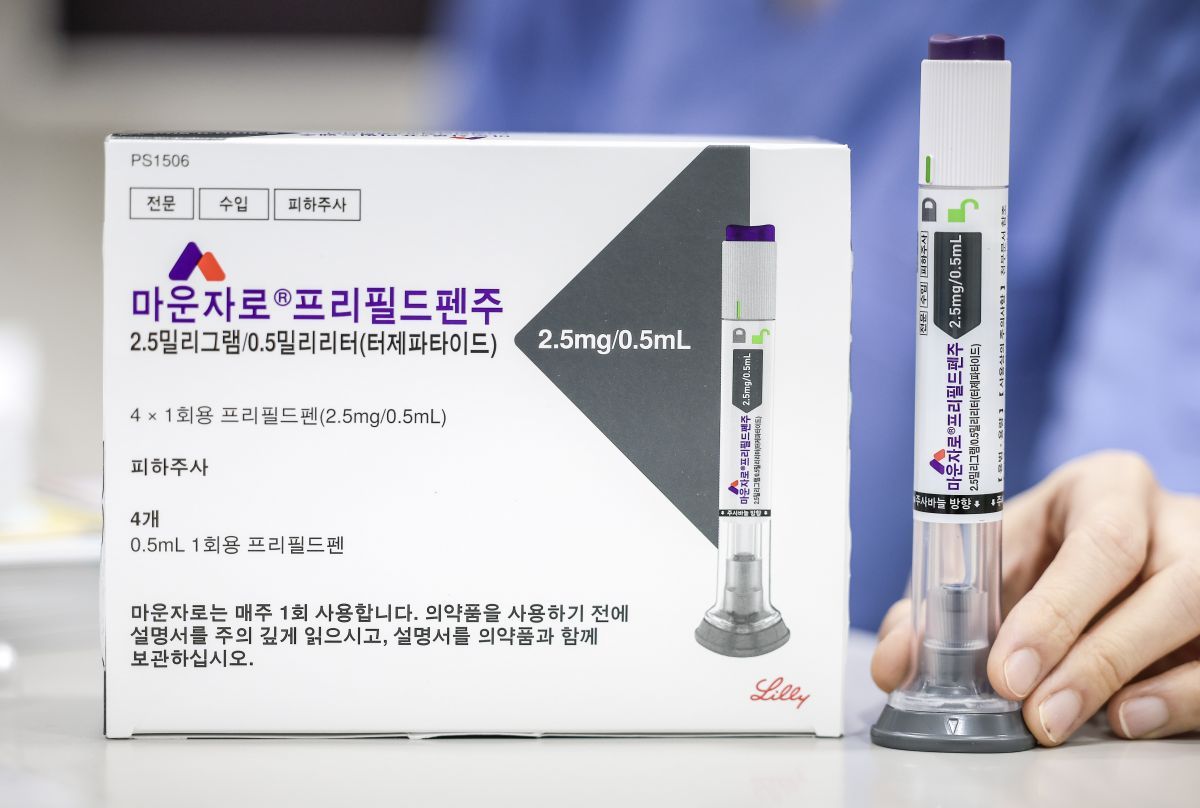
‘레카네맙(상품명 레켐비)’이 최근 식품의약품안전처 시판 허가를 받았다. 레카네맙은 초기 알츠하이머병이나 경도인지장애(치매 전 단계)의 질병 진행과 인지 기능 저하 속도를 늦춰 20년 만에 치매 신약으로 공식 인정받았다. 올해 말쯤 국내 환자들도 이 약을 쓸 수 있게 될 전망이다. 다만 약값이 연간 수천만원에 달해 신속한 건강보험 적용 등 환자 부담 경감책이 뒷받침돼야 한다는 목소리가 높다.
10일 제약·의료계에 따르면 지난달 24일 성인 환자 대상으로 승인받은 레카네맙은 알츠하이머병을 일으키는 뇌 속 독성물질 아밀로이드베타 응집체에 직접 작용하는 항체 치료제다. 3상임상시험 결과 1년 6개월 시점에 해당 약 투여군에서 위약군 대비 질병 진행(인지 기능 악화)이 27% 지연된 것으로 확인됐다. 경도인지장애 환자의 일상생활 기능 저하를 37% 늦추는 효과도 입증됐다. 다만 약 투여군에서 뇌부종과 뇌미세혈관 출혈 등의 이상 반응이 보고됐다.
권장 용량은 체중 1㎏당 10㎎으로 2주에 한 번씩 병원에서 1시간 동안 정맥 주사로 투여받는다(제약사는 주 1회 집에서 환자가 스스로 투여하는 주사제 개발 중). 치료 시작 전에 최근 1년 내 뇌 MRI 영상에서 아밀로이드베타 관련 이상이 존재하는지 확인해야 한다. 치료 기간에도 증상이 없는 부작용이 있는지 확인하기 위해 5, 7, 14차 투여 전 MRI 확인이 필요하다. 뇌부종 등이 확인되면 즉시 주사를 멈추고 치료 일정을 조정해야 한다.
레카네맙 이전에 개발됐던 아밀로이드베타 타깃 치료제 ‘아두카누맙’은 임상 참여자 약 41%에서 뇌출혈과 부종이 보고됐다. 미국 식품의약국(FDA) 조건부 승인에도 현재 시장 퇴출 수순을 밟고 있다.
비싼 약가는 문제다. 미국의 경우 연간 약 3500만원, 일본은 2700만원의 비용이 책정됐다. 한국에서도 비슷하거나 약간 낮은 가격으로 정해질 가능성이 있다.
한양대구리병원 신경과 최호진 교수는 “고비용임에도 들어오면 치료받겠다는 환자들이 많다. 실제 일본 가서 맞고 온 이들도 있다. 일본은 정부 지원으로 최근 6개월간 4000~5000명이 맞았다고 한다. 치매 전문가들 기대도 크다”고 말했다. 최 교수는 “부작용 없는 약은 없다. FDA도 투약으로 인한 부작용보다 이익이 더 크다고 판단해 승인했다. 그렇더라도 부작용이 분명 존재하는 만큼, 처방 대상 환자를 조심스럽게 선별하고 어느 때 써야 할지 현재 학회 차원의 진료 가이드라인을 만들고 있다”고 덧붙였다.
민태원 의학전문기자 twmin@kmib.co.kr
GoodNews paper ⓒ 국민일보(www.kmib.co.kr), 무단전재, 수집, 재배포 및 AI학습 이용 금지